Molekulaarinen lääketiede
Johtajat
Tutkimusryhmän toiminta
Seppo Ylä-Herttualan Molekulaarisen lääketieteen tutkimusryhmän tavoitteena on kehittää uusia geeniterapiamuotoja sydän- ja verisuonitauteihin sekä pahanlaatuiseen aivosyöpään. Tutkimusryhmämme on ollut pitkään osana uraa uurtavaa geeniterapia-alan tutkimusta ja toteutimme ensimmäisenä maailmassa adenoviruksen siirron ihmisen verisuoneen vuonna 1996. Tärkeimpiin saavutuksiimme voidaan laskea VEGF-geeniterapian kehittäminen, VEGF-geeniperheen vähemmän tunnettujen jäsenten merkityksen karakterisointi veri- ja imusuonistossa sekä monien uusien sydän- ja verisuonitautien hoitojen kohdegeenien tunnistaminen.
”Meidän suurin vahvuutemme on mahdollisuus viedä geeniterapiainnovaatiot suoraan laboratoriosta klinikkaan. Meillä on tietämys ja tilat kehittämiemme uusien terapioiden testaamisen ensin pieneläin- ja isoeläinmalleissa ennen kliinisiä kokeita. Se, että Kansallinen virusvektorilaboratorio, in vitro ja in vivo laboratoriot sekä Kuopion yliopistollinen sairaala ovat samalla kampuksella, mahdollistaa täysin translationaalisen tutkimuksen”, professori Seppo Ylä-Herttuala kertoo.
Tähän mennessä Kansallisen virusvektorilaboratorion kehittämistä virusvektoreista kahdeksan on päätynyt faasin I/II/III kliinisiin kokeisiin. Vuosien saatossa kerätty kokemus ja kampuksen erinomainen infrastruktuuri mahdollistavat myös muiden virusvektoreiden käyttöön pohjautuvien innovaatioiden nopean kehityksen, kuten tällä hetkellä tuottamamme koronarokote maailmalla riehuvaa pandemiaa vastaan. Tutkimusaiheemme vaihtelevat virusvektoreista kliinisiin kokeisiin, joten ryhmässä on paljon erilaisten aihepiirien asiantuntemusta.
UEFin yhteistyökumppanit
Yhteistyö
-
 Kardiovaskulaarinen Genomiikka (Kaikkonen tutkimusryhmä) 01.09.2015 -
Kardiovaskulaarinen Genomiikka (Kaikkonen tutkimusryhmä) 01.09.2015 - -
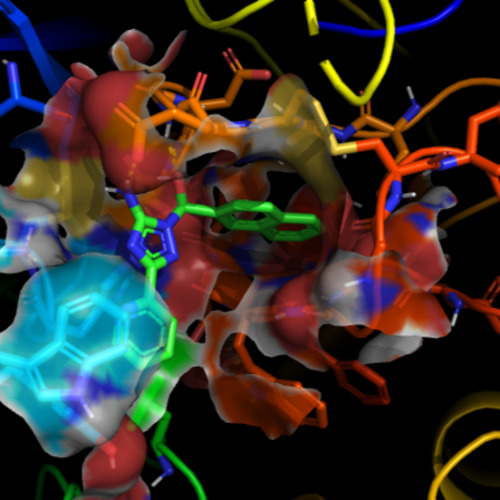 Molekyylimallinnuksen ja lääkeainesuunnittelun tutkimusryhmä 01.01.2010 -
Molekyylimallinnuksen ja lääkeainesuunnittelun tutkimusryhmä 01.01.2010 - -
 Silmälääketutkimusryhmä 01.01.2010 -
Silmälääketutkimusryhmä 01.01.2010 - -
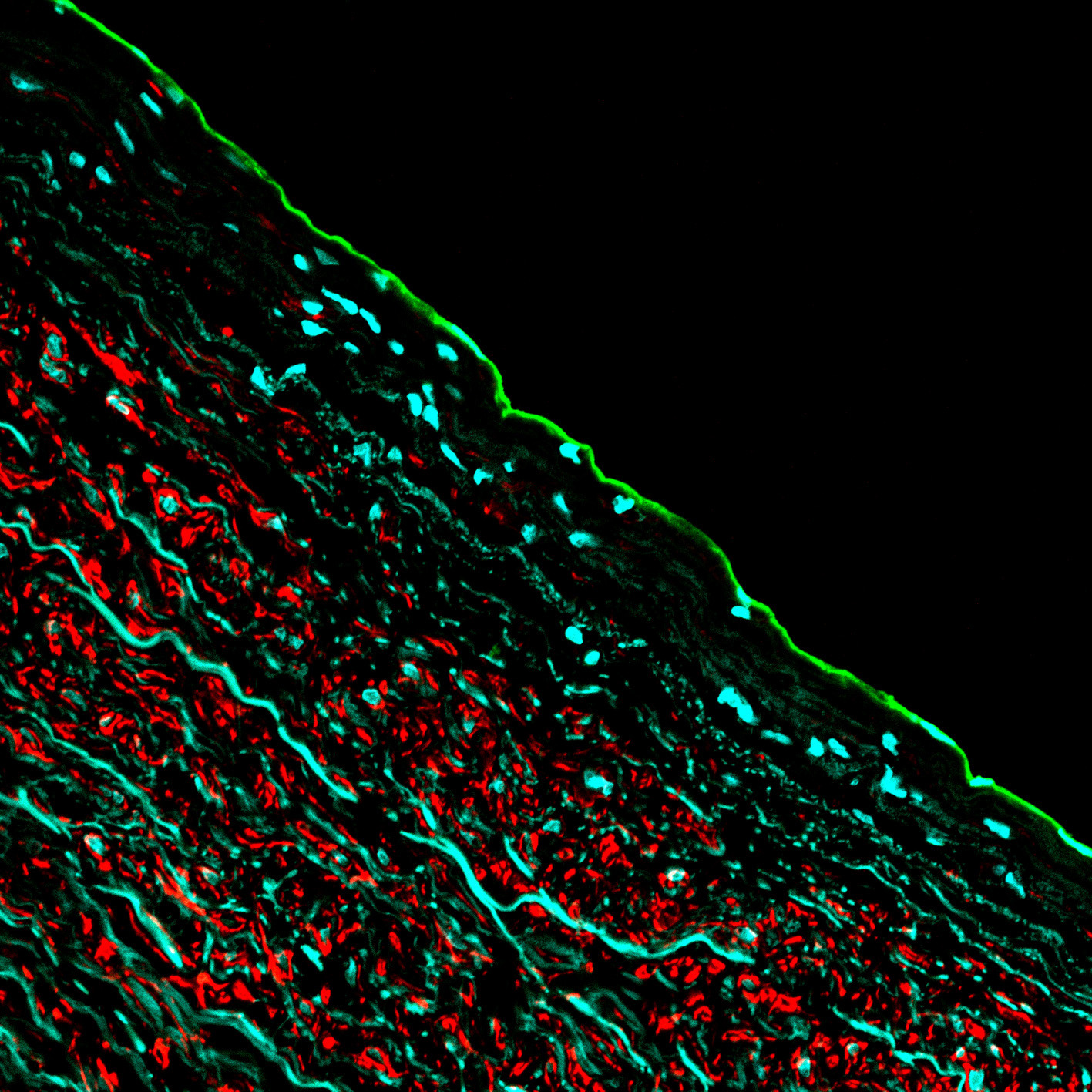 Verisuonibiologian tutkimusryhmä (Laakkonen) 01.09.2019 -
Verisuonibiologian tutkimusryhmä (Laakkonen) 01.09.2019 - -
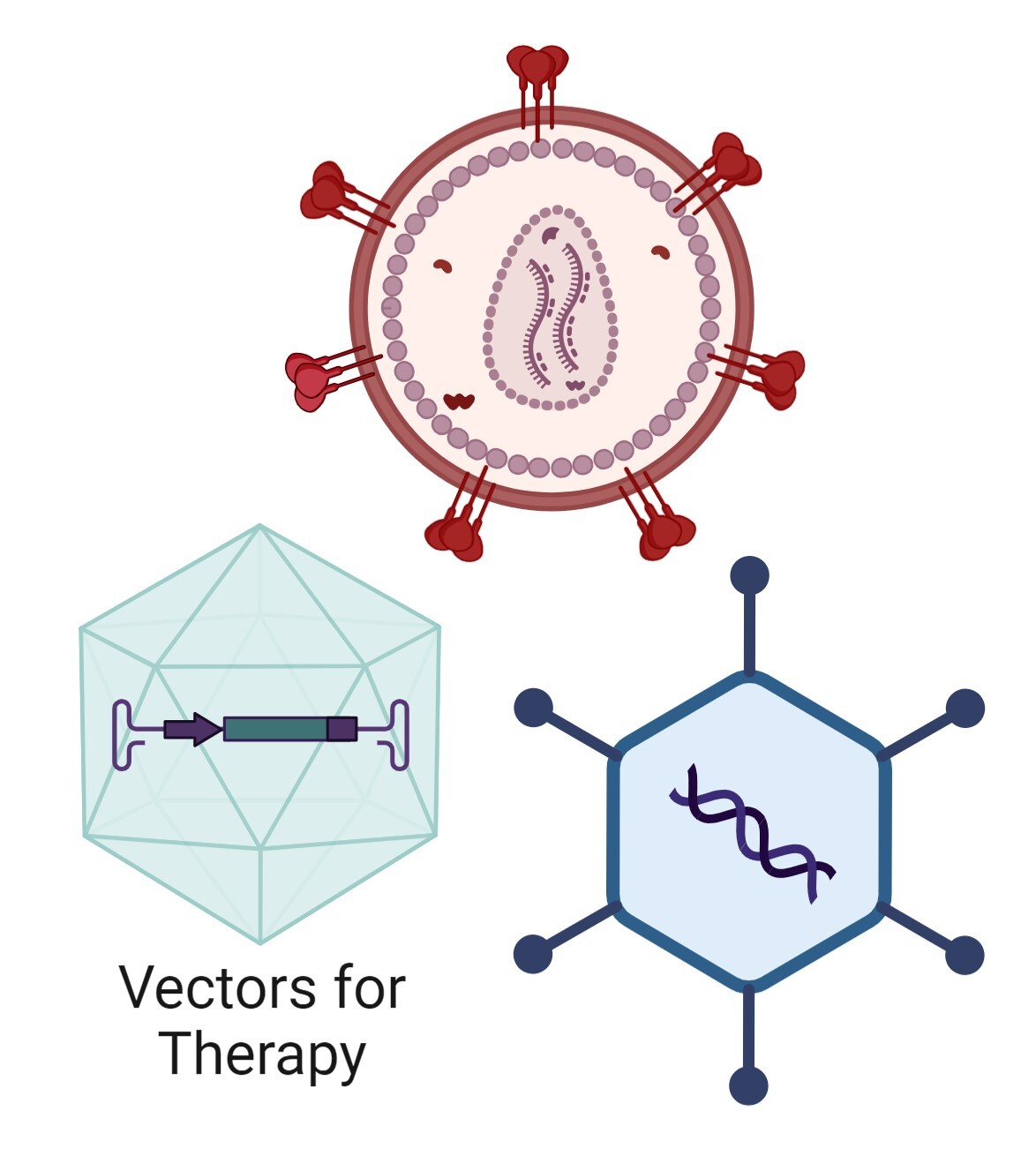 Translationaalinen Vektoritutkimus 01.01.2024 -
Translationaalinen Vektoritutkimus 01.01.2024 -
Projektit
-
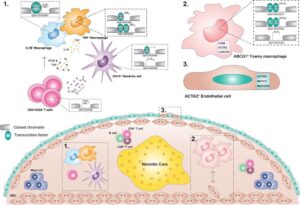
Human atherosclerotic plaque microanatamical characterisation using single-cell transcriptomics (Depuydt et al 2020) Histopatologista analyysia ja erilaisia kuvantamistekniikoita (esim. MRI, IVUS, TT) on käytetty valtimoiden seinien muutosten etsimiseen ja ateroskleroottisten vaurioiden muodostumisen tutkimiseen. Histopatologisilla menetelmillä muutoksia voidaan tutkia yksittäisten solujen tasolla, mutta nämä menetelmät ovat rajoittuneet pieneen määrään markkereita kerrallaan (3-5 proteiinia ja/tai mRNA:ta). Markkereiden rajoitetun määrän takia näillä menetelmillä ei pystytä erottelemaan hienovaraisia eroja solujen fenotyypeissä. Kuvantamistekniikat ovat noninvasiivisia, mutta niiden resoluutio on liian alhainen yksittäisten solujen tutkimiseen. Ateroskleroottisten vaurioiden mikroanatomian tutkimiseen tarvitaan siis lisäksi uudempia tekniikoita. Moderni rinnakkaissekvensointi yhden solun RNA:sta (scRNA-seq) mahdollistaa satojen transkriptien tunnistamisen yksittäisistä soluista, mutta tällä menetelmällä ei saada tietoa solujen sijainnista kudoksessa. Paikkatranskriptomiikan tekniikat sen sijaan määrittävät tarkasti transkriptien sijainnin kudoksessa, mutta niillä ei pystytä määrittämään solutyyppiä, josta nämä transkriptit ovat peräisin. Tavoitteenamme on yhdistää scRNA-sekvensointidatan ja paikkatranskriptomiikan vahvuudet ateroskleroottisten vaurioiden mikroanatomian tutkimuksessa. Näiden menetelmien tuottaman datan yhdistäminen mahdollistaa solujen biologisen identiteetin ja sijainnin selvittämisen. Tuoreessa julkaisussa (Depuydt et al 2020) selvitimme ihmisen ateroskleroottisista vaurioista löytyvien 14 eri solutyypin molekulaariset ominaisuudet scRNA-seq-analyysilla. Tuhansien yksittäisten solujen molekulaarinen profilointi on mahdollistanut sellaisten markkereiden valitsemisen, joilla pystytään paikallistamaan ja kvantitoimaan solutyypit, jotka kommunikoivat keskenään erityyppisissä ateroskleroottisissa vaurioissa. Laajennusmikroskopia (engl. expansion microscopy) on uusi menetelmä paikkatranskriptomiikassa, ja sen avulla voidaan erottaa kymmeniä ja jopa satoja ilmennettyjä geenejä samanaikaisesti kudosnäytteestä käyttämättä superresoluutiomikroskooppia. Projektissa mukana
Yhteistyökumppanit
Julkaisuja
- Depuydt MAC, Prange KHM, Slenders L, Örd T, Elbersen D, Boltjes A, de Jager SCA, Asselbergs FW, de Borst GJ, Aavik E, Lönnberg T, Lutgens E, Glass CK, den Ruijter HM, Kaikkonen MU, Bot I, Slütter B, van der Laan SW, Yla-Herttuala S, Mokry M, Kuiper J, de Winther MPJ, Pasterkamp G. Microanatomy of the Human Atherosclerotic Plaque by Single-Cell Transcriptomics. Circ Res. 2020 Nov 6;127(11):1437-1455.
-
 Suomen Akatemian rahoittamassa COVID-19-rokotekehitysprojektissa tavoitteenamme on kehittää adenovirusvektoripohjainen rokote SARS-CoV-2-virusta vastaan. Adenovirusvektori ilmentää osaa viruksen piikkiproteiinista. Kun rokote annetaan nenäsumutteena, sen odotetaan tuottavan vahvan immuunivasteen virukselle. Projektissa mukana
Suomen Akatemian rahoittamassa COVID-19-rokotekehitysprojektissa tavoitteenamme on kehittää adenovirusvektoripohjainen rokote SARS-CoV-2-virusta vastaan. Adenovirusvektori ilmentää osaa viruksen piikkiproteiinista. Kun rokote annetaan nenäsumutteena, sen odotetaan tuottavan vahvan immuunivasteen virukselle. Projektissa mukana- Ahmed Tawfek, Aino Sormunen, Erika Gurzeler-Tiihonen, Nihay Laham-Karam, Petri Mäkinen, Seppo Ylä-Herttuala
Yhteistyökumppanit
-
Tutkimme pahanlaatuisia aivokasvaimia. Glioblastoomaan keskittyvissä projekteissamme selvitämme sen ominaispiirteitä ja pyrimme löytämään uusia syövän merkkiaineita. Lisäksi mallinnamme sairautta monipuolisin lähestymistavoin erityisesti potilasperäisen materiaalin avulla. Tutkimme myös uusia immunoterapeuttisia hoitoja. Merkkiaineista saatava tieto voi hyödyttää potilasdiagnostiikkaa ja auttaa valitsemaan parempia ja henkilökohtaisempia hoitoja tulevaisuudessa.
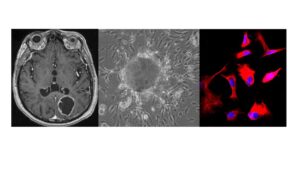
Magneettiresonanssikuva glioblastoomapotilaasta ennen leikkausta (muokattu Niittykoski ym. 2017), potilaasta eristettyjä glioomasoluja viljelmässä ja värjättyjä potilaasta eristettyjä glioomasoluja. Projektissa mukana
- Venla Olsson, Alisa Nousiainen,Suvi Shemeikka Minna Niittykoski, Seppo Ylä-Herttuala
Yhteistyökumppanit
- Vincenzo Cerullo (Helsingin yliopisto), Dario Greco (Tampereen yliopisto), Antti Huotarinen (Kuopion yliopistollinen keskussairaala), and Collaborators Susanna Rantala (Kuopio University Hospital)
Julkaisuja
- Olsson V, Niittykoski M, Stedt H, Virsunen H, Ylä-Herttuala S: Pahanlaatuisen gliooman hoidon tulevaisuuden näkymiä. Duodecim, 136: 1242-1248, 2020
- Niittykoski M, von und zu Fraunberg M, Martikainen M, Rauramaa T, Immonen A, Koponen S, Leinonen V, Vähä-Koskela M, Zhang Q, Kühnel F, Mei Y-F, Ylä-Herttuala S, Jääskeläinen JE, Hinkkanen A: Immunohistochemical characterization and sensitivity to human adenovirus serotypes 3, 5 and 11p of new cell lines derived from human diffuse grade lI-IV grade gliomas. Transl Oncol., 10: 772-779, 2017
-
 Keskitymme uusien hoitomuotojen kehitykseen – toimimme väylänä tutkimuslaboratoriosta klinikkaan.Kehitämme uusia sydän- ja verisuonisairauksien tautimalleja (kuten sydänlihasiskeamian ja sydämen vajaatoiminnan eläinmalli), joita hyödynnämme tutkimuksessamme. Käytämme uusimpia kuvantamismenetelmiä, kuten angiografiatutkimusta ja PET-kuvantamista yhteistyössä Kuopion yliopistollisen sairaalan kanssa. Lisäksi tutkimme kehittämiemme sydänlihaksen virusvektorivälitteisten geeniterpioiden antotapoja, tehokkuutta ja soveltuvuutta suurissa eläinmalleissa. Projektissa mukana
Keskitymme uusien hoitomuotojen kehitykseen – toimimme väylänä tutkimuslaboratoriosta klinikkaan.Kehitämme uusia sydän- ja verisuonisairauksien tautimalleja (kuten sydänlihasiskeamian ja sydämen vajaatoiminnan eläinmalli), joita hyödynnämme tutkimuksessamme. Käytämme uusimpia kuvantamismenetelmiä, kuten angiografiatutkimusta ja PET-kuvantamista yhteistyössä Kuopion yliopistollisen sairaalan kanssa. Lisäksi tutkimme kehittämiemme sydänlihaksen virusvektorivälitteisten geeniterpioiden antotapoja, tehokkuutta ja soveltuvuutta suurissa eläinmalleissa. Projektissa mukana- Juho Pajula, Jaakko Lampela, Jonna Räisänen, Niko Järveläinen, Satu Siimes, Minja Heikkilä, Anni Määttä, Hanna Wang, Peteri Mäkinen, Seppo Ylä-Herttuala
Yhteistyökumppanit
- Kuopion yliopistollinen sairaala, PET-keskus (TYKS)
Julkaisuja
- Pajula, J. J., Halonen, P. J., Hätinen, O. P., Ylä-Herttuala, S., & Nurro, J. (2020). Adenoviral Gene Transfer of Gremlin Modulates Vascular Endothelial Growth Factor-A-Induced Angiogenesis in Porcine Myocardium. Human Gene Therapy, 31(3–4), 211–218.
- Lähteenvuo J., Hätinen, O. P., Kuivanen, A., Huusko, J., Paananen, J., Lähteenvuo, M., … Ylä-Herttuala, S. (2020). Susceptibility to Cardiac Arrhythmias and Sympathetic Nerve Growth in VEGF-B Overexpressing Myocardium. Molecular Therapy, 28(7), 1731–1740.
- Hätinen, O. P. A., Lähteenvuo, J. E., Korpela, H. J., Pajula, J. J., & Ylä-Herttuala, S. (2019). Isolation of fresh endothelial cells from porcine heart for cardiovascular studies: A new fast protocol suitable for genomic, transcriptomic and cell biology studies. BMC Molecular and Cell Biology, 20(1).
-
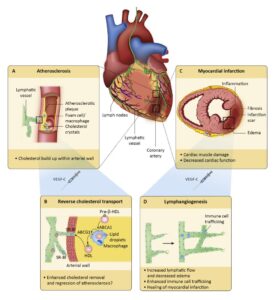 Hiiri on tärkeä eläinmalli ihmisten sydän- ja verisuonitauteja tutkittaessa genomin samankaltaisuutensa ja nopean lisääntymistahtinsa vuoksi. Käyttämämme hiirimallit sisältävät useita sydän- ja veritautimalleja, kuten ateroskleroosin, sydämen vajaatoiminnan ja iskeemisten sydänsairauksien tautimallit. Näiden lisäksi käytämme pieneläinmalleja rasva-aineenvaihdunnan, silmän uudissuonimuodostuksen ja kakkostyypin diabetekseen liittyvien kardiovaskulaaristen komplikaatioiden tutkimiseen. Pyrimme selvittämään näiden sairauksien etenemistä ja kehittämään niihin uusia geeniterapioita. Projektissa mukana
Hiiri on tärkeä eläinmalli ihmisten sydän- ja verisuonitauteja tutkittaessa genomin samankaltaisuutensa ja nopean lisääntymistahtinsa vuoksi. Käyttämämme hiirimallit sisältävät useita sydän- ja veritautimalleja, kuten ateroskleroosin, sydämen vajaatoiminnan ja iskeemisten sydänsairauksien tautimallit. Näiden lisäksi käytämme pieneläinmalleja rasva-aineenvaihdunnan, silmän uudissuonimuodostuksen ja kakkostyypin diabetekseen liittyvien kardiovaskulaaristen komplikaatioiden tutkimiseen. Pyrimme selvittämään näiden sairauksien etenemistä ja kehittämään niihin uusia geeniterapioita. Projektissa mukana- Sanna Kettunen, Erika Gurzeler, Anna-Kaisa Ruotsalainen, Rahul Mallick, Sanna Koponen, Krista Hokkanen, Diana Törmä, Anna Slita, ja Seppo Ylä-Herttuala
Julkaisuja
- Gurzeler E, Aavik E, Laine A, Valkama T, Niskanen H, Huusko J, Kaikkonen MU, Ylä-Herttuala S. Therapeutic effects of rosuvastatin in hypercholesterolemic prediabetic mice in the absence on low density lipoprotein receptor. Biochim Biophys Acta Gen Sub. 2019 Feb;1863(2):481-490.
- Tirronen A, Vuorio T, Kettunen S, Hokkanen K, Ramms B, Niskanen H, Laakso H, Kaikkonen MU, Jauhiainen M, Gordts PLSM, Ylä-Herttuala S. Deletion of lymphangiogenic and angiogenic growth factor VEGF-D leads to severe hyperlipidemia and delayed clearance of chylomicron remnants. Arterioscler Thromb Vasc Biol. 2018 Oct;38(10):2327-2337.
- Kokki E, Karttunen T, Olsson V, Kinnunen K, Ylä-Herttuala S. Human vascular endothelial growth factor A(165) expression induces the mouse model of neovascular age-related macular degeneration. Genes (Basel). 2018 Aug 31;9(9):438.
- Devi D, Babu M, Mäkinen P, Kaikkonen MU, Heinäniemi M, Laakso H, Ylä-Herttuala E, Rieppo L, Liimatainen T, Naumenko N, Tavi P, Ylä-Herttuala S. Aggravated Postinfarct Heart Failure in Type 2 Diabetes Is Associated with Impaired Mitophagy and Exaggerated Inflammasome Activation. Am J Pathol. 2017 Dec;187(12):2659-2673.
-
 Virusvektorit ovat tehokkaita työkaluja geeniterapiassa ja tutkimuskäytössä. Niiden parantamiseksi olemme hyödyntäneet ei-koodaavaa RNA:ta ja ei-koodaavaa genomia, kuten supertehostimia, kehittääksemme solutyyppeihin kohdennettuja vektoreita ja endogeenisten geenien ilmentymistä sääteleviä vektoreita. Verisuonet rakentuvat endoteelisoluista, joten terapeuttisten vektoreiden kohdentaminen näihin soluihin olisi hyödyllistä angiogeenisen geeniterapian kannalta. Siksi olemme tutkineet supertehostimia, joilla voisimme rajata siirtogeenien ilmentymisen vain endoteelisoluihin. Olemme löytäneet tehostimen, jonka avulla voimme ilmentää siirtogeenejä vain endoteelisoluissa. Lisäksi CRISPR/Cas9-tekniikkaa hyödyntämällä olemme muokanneet tehostimia ja löytäneet aiemmin tuntemattomia välittäjiä verisuonten muodostuksessa. Olemme tuottaneet endoteelisoluihin kohdennettuja vektoreita ja osoittaneet, miten vastaavia vektoreita voidaan kohdentaa myös muihin solutyyppeihin. Jatkossa tutkimme mm. endoteeli- ja hypoksiaspesifistä sirkulaarista RNA:ta. Tämä on ei-koodaavan RNA:n muoto, jolla voi olla merkittävä rooli geenien säätelyssä, ja joka voi avata uusia mahdollisuuksia geeniterapiaan. Projektissa mukana
Virusvektorit ovat tehokkaita työkaluja geeniterapiassa ja tutkimuskäytössä. Niiden parantamiseksi olemme hyödyntäneet ei-koodaavaa RNA:ta ja ei-koodaavaa genomia, kuten supertehostimia, kehittääksemme solutyyppeihin kohdennettuja vektoreita ja endogeenisten geenien ilmentymistä sääteleviä vektoreita. Verisuonet rakentuvat endoteelisoluista, joten terapeuttisten vektoreiden kohdentaminen näihin soluihin olisi hyödyllistä angiogeenisen geeniterapian kannalta. Siksi olemme tutkineet supertehostimia, joilla voisimme rajata siirtogeenien ilmentymisen vain endoteelisoluihin. Olemme löytäneet tehostimen, jonka avulla voimme ilmentää siirtogeenejä vain endoteelisoluissa. Lisäksi CRISPR/Cas9-tekniikkaa hyödyntämällä olemme muokanneet tehostimia ja löytäneet aiemmin tuntemattomia välittäjiä verisuonten muodostuksessa. Olemme tuottaneet endoteelisoluihin kohdennettuja vektoreita ja osoittaneet, miten vastaavia vektoreita voidaan kohdentaa myös muihin solutyyppeihin. Jatkossa tutkimme mm. endoteeli- ja hypoksiaspesifistä sirkulaarista RNA:ta. Tämä on ei-koodaavan RNA:n muoto, jolla voi olla merkittävä rooli geenien säätelyssä, ja joka voi avata uusia mahdollisuuksia geeniterapiaan. Projektissa mukana- Tuisku Suoranta, Maria Barbiera, Aino Sormunen, Theodore Boc, Anni Herrala, Mari Mäkelä, Nihay Laham-Karam, Seppo Ylä-Herttuala
Yhteistyökumppanit
- Johanna Laakkonen, Adam Whaley-Connell, Elias Ylä-Herttuala
Julkaisuja
- Mushimiyimana I, Niskanen H, Beter M, Laakkonen JP, Kaikkonen M, Ylä-Herttuala S., Laham-Karam N. Discovery and characterisation of functional endothelial super-enhancers. Nucleic Acids Research. 2021; 20;49(14):8078-8096.
- Mushimiyimana I, Tomas Bosch V, Niskanen H, Downes N, Ylä-Herttuala S, Laham-Karam N, Kaikkonen M. Genomic landscapes of VEGF family members in endothelial cells. Molecular and Cellular Biology 41(7): e0059420.
- Suoranta T, Laham-Karam N, Ylä-Herttuala S. Optimised protocol for accurate titration of AAV vectors. Human Gene Therapy. 2021;32(19-20).
-
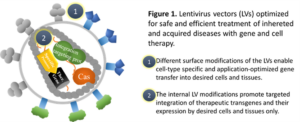 Tutkimuksemme kohteena on turvallisten ja tehokkaiden geenikuljettimien kehittäminen ja käyttö geeniterapiassa. Tavoitteenamme on hoitaa erilaisia sairauksia, kuten sydämen vajaatoimintaa ja familiaalista hyperkolesterolemiaa. Pyrimme myös tuottamaan turvallisia ja mahdollisimman tehokkaita CAR T-soluja soluterapiakäyttöön. Työkaluinamme käytämme pääasiassa lentivirusvektoreita, joita olemme muokanneet monella tasolla sopivammiksi geeniterapiatyökaluiksi. Vektorien pintamuokkauksella geeninsiirto rajoitetaan vain niihin solu- ja kudostyyppeihin, joissa geeniterapiaa tarvitaan, ja terapeuttisten geenien kohdennettu integraatio turvallisille alueille perimässä pienentää haitallisten mutaatioiden riskiä. Nämä muutokset vähentävät geeniterapian mahdollisia sivuvaikutuksia, ja näin parantavat geeniterapian turvallisuutta. Muokattujen lentivirusvektoreiden lisäksi käytämme myös CRISPR/Cas-tekniikkaa mm. kohdennettuun integraatioon. Tuoreimmassa julkaisussamme tutkimme, kuinka endonukleaasin lisääminen lentivirusvektorin integraatiojärjestelmään vaikuttaa siirtogeenin sijaintiin solun perimässä. Osoitimme, että endonukleaasin sisältävät vektorit eivät integroidu proteiineja koodaaviin geeneihin samalla tavalla kuin villityypin vektorit, vaan siirtogeenit kohdentuivat tavoitealueelle yli 20 % tehokkuudella (Schenkwein et al, 2020). Projektissa mukana
Tutkimuksemme kohteena on turvallisten ja tehokkaiden geenikuljettimien kehittäminen ja käyttö geeniterapiassa. Tavoitteenamme on hoitaa erilaisia sairauksia, kuten sydämen vajaatoimintaa ja familiaalista hyperkolesterolemiaa. Pyrimme myös tuottamaan turvallisia ja mahdollisimman tehokkaita CAR T-soluja soluterapiakäyttöön. Työkaluinamme käytämme pääasiassa lentivirusvektoreita, joita olemme muokanneet monella tasolla sopivammiksi geeniterapiatyökaluiksi. Vektorien pintamuokkauksella geeninsiirto rajoitetaan vain niihin solu- ja kudostyyppeihin, joissa geeniterapiaa tarvitaan, ja terapeuttisten geenien kohdennettu integraatio turvallisille alueille perimässä pienentää haitallisten mutaatioiden riskiä. Nämä muutokset vähentävät geeniterapian mahdollisia sivuvaikutuksia, ja näin parantavat geeniterapian turvallisuutta. Muokattujen lentivirusvektoreiden lisäksi käytämme myös CRISPR/Cas-tekniikkaa mm. kohdennettuun integraatioon. Tuoreimmassa julkaisussamme tutkimme, kuinka endonukleaasin lisääminen lentivirusvektorin integraatiojärjestelmään vaikuttaa siirtogeenin sijaintiin solun perimässä. Osoitimme, että endonukleaasin sisältävät vektorit eivät integroidu proteiineja koodaaviin geeneihin samalla tavalla kuin villityypin vektorit, vaan siirtogeenit kohdentuivat tavoitealueelle yli 20 % tehokkuudella (Schenkwein et al, 2020). Projektissa mukanaYhteistyökumppanit
Julkaisuja
- Schenkwein D, Afzal S, Nousiainen A, Schmidt M, Ylä-Herttuala S. Efficient Nuclease-Directed Integration of Lentivirus Vectors into the Human Ribosomal DNA Locus. Mol Ther. 2020 Aug 5;28(8):1858-1875. doi: 10.1016/j.ymthe.2020.05.019. Epub 2020 May 23. PMID: 32504545; PMCID: PMC7403359.
-
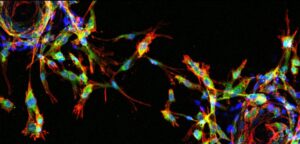 Tutkimusryhmämme (eng. junior research group) keskittyy sydän- ja verisuonitautien hoitojen kehittämiseen. Tutkimuksessamme selvitämme tautimekanismeja sekä solujen välisiä vuorovaikutussuhteita ja tunnistamme potentiaalisia uusia hoitogeenejä. Tuoreessa julkaisussamme osoitimme ensimmäistä kertaa, että kasvutekijä BMP-6 vaikuttaa verisuonten uudismuodostukseen ja säätelee VEGFR2/Hippo-soluviestintäreittiä. Löydöstä voidaan hyödyntää verisuonten kasvua säätelevien hoitomuotojen kehityksessä. Projektissa mukana
Tutkimusryhmämme (eng. junior research group) keskittyy sydän- ja verisuonitautien hoitojen kehittämiseen. Tutkimuksessamme selvitämme tautimekanismeja sekä solujen välisiä vuorovaikutussuhteita ja tunnistamme potentiaalisia uusia hoitogeenejä. Tuoreessa julkaisussamme osoitimme ensimmäistä kertaa, että kasvutekijä BMP-6 vaikuttaa verisuonten uudismuodostukseen ja säätelee VEGFR2/Hippo-soluviestintäreittiä. Löydöstä voidaan hyödyntää verisuonten kasvua säätelevien hoitomuotojen kehityksessä. Projektissa mukana- Henna Ilmonen, Miika Kiema, Emma Luoto, Heidi Pulkkinen, Heta Rasinkangas, Mustafa Beter, Suvi Jauhiainen, Johanna Laakkonen
Julkaisuja
- Pulkkinen HH, Kiema M, Lappalainen JP, Toropainen A, Beter M, Tirronen A, Holappa L, Niskanen H, Kaikkonen MU, Ylä-Herttuala S, Laakkonen JP. BMP6/TAZ-Hippo signaling modulates angiogenesis and endothelial cell response to VEGF. Angiogenesis. 2020 Oct 6. doi:10.1007/s10456-020-09748-4.
Rahoitus
-









-
Decision: 337120

 Grant ID: 825670 Grant ID: 884382
Grant ID: 825670 Grant ID: 884382 
 Grant ID: 731532
Grant ID: 731532  Grant ID: 945473
Grant ID: 945473  Euro GCT Grant ID: 965241
Euro GCT Grant ID: 965241
Johtajat
Vanhemmat tutkijat
-

Nihay Laham Karam
TutkimusjohtajaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Johanna Laakkonen
Apulaisprofessori (Associate Professor)A.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Petri Mäkinen
Staff ScientistA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Minna Niittykoski
YliopistotutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Diana Schenkwein
YliopistotutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Erika Gurzeler-Tiihonen
TutkijatohtoriA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Tiina Nieminen
TutkimuspäällikköA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Minna Karhinen
YliopistonlehtoriFarmasian laitos, Terveystieteiden tiedekunta -
Vesa Turkki
TutkimuspäällikköA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Anna-Kaisa Ruotsalainen
YliopistotutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Suvi Jauhiainen
ProjektitutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Jarkko Hytönen
YliopistotutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta
Tutkijatohtorit
-

Venla Olsson
AluepäällikköA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Alisa Nousiainen
TutkijatohtoriA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Mustafa Beter
TutkijatohtoriA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Heidi Pulkkinen
TutkijatohtoriA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Sanna Koponen
TutkijatohtoriA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Sanna Kettunen
TutkijatohtoriA.I. Virtanen -instituutti, Terveystieteiden tiedekunta
Väitöskirjatutkijat
-

Maria Barbiera
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Theodor Boc
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Guillem Buesa Maes
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Pracheta De
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Minja Heikkilä
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Krista Hokkanen
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Greta Juusola
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Miika Kiema
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Riku Kiviluoto
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Miia Kulmala
ProjektitutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Anni Herrala
ProjektitutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Jaakko Lampela
Vieraileva tutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Rahul Mallick
ApurahatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Anni Määttä
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Iida Räty
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Satu Siimes
ApurahatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Anna Slita
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Aino Sormunen
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Tuisku Suoranta
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Diana Törmä
VäitöskirjatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Hanna Wang
TutkimusavustajaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta
Teknikot
-
Sari Järveläinen
ErikoislaboratoriomestariA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Tiina Koponen
ErikoislaboratoriomestariA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Maarit Mähönen
LaboratoriomestariA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Sonja Kotoneva
LaboratorioteknikkoA.I. Virtanen -instituutti, Terveystieteiden tiedekunta
Tukihenkilöstö
-
Svetlana Laidinen
ProjektitutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -

Ahmed Tawfek
ProjektitutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta
Jatko-opiskelija
-
Jarkko Kuivalainen
TutkimusavustajaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Liinu Kilpeläinen
ProjektitutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Eveliina Aarnio
ApurahatutkijaA.I. Virtanen -instituutti, Terveystieteiden tiedekunta -
Mari Mäkelä
OpetusavustajaBiolääketieteen yksikkö, Lääketieteen laitos, Terveystieteiden tiedekunta

